Eosinófilos en el penfigoide ampolloso: una revisión narrativa
DOI:
https://doi.org/10.29176/2590843X.1998Palabras clave:
Dermatosis ampollar, penfigoide ampolloso, eosinófilos, Inmunoglobulina E, fisiopatologíaResumen
El penfigoide ampolloso (PA) es una enfermedad ampollosa autoinmune que afecta principalmente a adultos mayores, con una incidencia que varía de 2.4 a 42.8 casos por millón de habitantes-año. En Colombia, se encuentra entre las enfermedades ampollosas autoinmunes más comunes, y la mayoría de los pacientes son mujeres mayores de 70 años. La enfermedad se manifiesta con ampollas tensas sobre placas eritematosas o urticariformes, principalmente en tronco y flexuras, y puede involucrar mucosas en el 10-30% de los casos. El diagnóstico se basa en características clínicas y pruebas paraclínicas, como histopatología e inmunofluorescencia. Se ha asociado una mayor severidad y mortalidad con altos recuentos de eosinófilos en los tejidos.
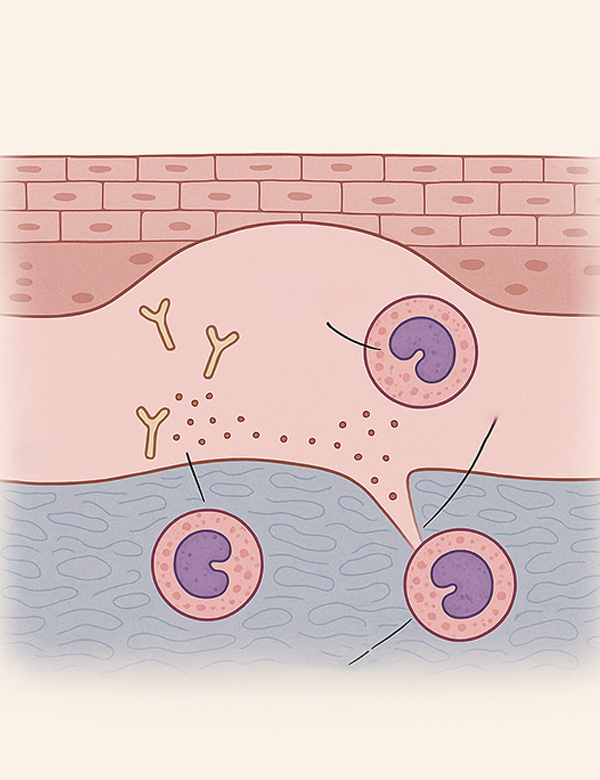
Los eosinófilos, granulocitos presentes en bajos niveles en condiciones normales, pueden aumentar en enfermedades alérgicas e infecciosas. En el PA, juegan un papel crucial al mediar la formación de ampollas mediante la degranulación, que degrada la membrana basal. La patogenia del PA involucra autoanticuerpos contra componentes de hemidesmosomas, como BP180, y la activación del complemento que recluta eosinófilos. La IgE también desempeña un papel importante en la activación de eosinófilos.
El tratamiento clásico incluye glucocorticoides y, en algunos casos, terapias inmunosupresoras. Las opciones biológicas como rituximab, omalizumab y dupilumab han mostrado beneficios, especialmente en casos refractarios. Nuevas terapias dirigidas a eosinófilos y sus vías están en estudio, con prometedores resultados preliminares. El conocimiento del rol de los eosinófilos en el PA está llevando al desarrollo de tratamientos más específicos y efectivos.
Biografía del autor/a
Artur Moraes-L'Abbate, Pontificia Universidad Javeriana, Bogotá, Colombia
Residente de Dermatología, Pontificia Universidad Javeriana, Bogotá, Colombia
Carolina Cortés Correa, Hospital Universitario de la Samaritana, Bogotá, Colombia
Dermatóloga, Hospital Universitario de la Samaritana, Bogotá, Colombia.
Referencias bibliográficas
Lu L, Chen L, Xu Y, Liu A. Global incidence and prevalence of bullous pemphigoid: A systematic review and meta-analysis. J Cosmet Dermatol 2022 -10;21(10):4818-4835.
Amber KT, Murrell DF, Schmidt E, Joly P, Borradori L. Autoimmune Subepidermal Bullous Diseases of the Skin and Mucosae: Clinical Features, Diagnosis, and Management. Clin Rev Allergy Immunol 2018 -02;54(1):26-51.
Ximena Alexandra Pinilla Garcia. Estudio de las características clínicas y epidemiológicas de los pacientes con enfermedades ampollosas autoinmunes en un hospital de tercer nivel de Bogotá Universidad Nacional de Colombia; 2015.
Zuluaga DC, Del Río DY, Úsuga YA, Aguirre-Acevedo D, Velásquez MM. Estudio retrospectivo clínico-epidemiológico de los pacientes con pénfigo y penfigoide ampolloso del Hospital Universitario San Vicente Fundación. Rev Asoc Colomb Dermatol Cir Dematol 2017;25(2):118-129.
Kayani M, Aslam AM. Bullous pemphigoid and pemphigus vulgaris. BMJ 2017 -06-08;357:j2169.
Miyamoto D, Santi CG, Aoki V, Maruta CW. Bullous pemphigoid. An Bras Dermatol 2019;94(2):133-146.
Lamberts A, Meijer JM, Jonkman MF. Nonbullous pemphigoid: A systematic review. J Am Acad Dermatol 2018 -05;78(5):989-995.e2.
Gore Karaali M, Koku Aksu AE, Cin M, Leblebici C, Kara Polat A, Gurel MS. Tissue eosinophil levels as a marker of disease severity in bullous pemphigoid. Australas J Dermatol 2021 -05;62(2):e236-e241.
Davoine F, Lacy P. Eosinophil Cytokines, Chemokines, and Growth Factors: Emerging Roles in Immunity. Front Immunol 2014 -11-10;5:570.
Marichal T, Mesnil C, Bureau F. Homeostatic Eosinophils: Characteristics and Functions. Front Med (Lausanne) 2017;4:101.
Jung Y, Rothenberg ME. Roles and regulation of gastrointestinal eosinophils in immunity and disease. J Immunol 2014 -08-01;193(3):999-1005.
Rothenberg ME, Hogan SP. The eosinophil. Annu Rev Immunol 2006;24:147-174.
Akuthota P, Wang H, Weller PF. Eosinophils as Antigen-Presenting Cells in Allergic Upper Airway Disease. Curr Opin Allergy Clin Immunol 2010 -2;10(1):14-19.
Bağcı IS, Horváth ON, Ruzicka T, Sárdy M. Bullous pemphigoid. Autoimmun Rev 2017 -05;16(5):445-455.
Liu Y, Li L, Xia Y. BP180 Is Critical in the Autoimmunity of Bullous Pemphigoid. Front Immunol 2017;8:1752.
Hertl M, Eming R, Veldman C. T cell control in autoimmune bullous skin disorders. J Clin Invest 2006 -5-1;116(5):1159-1166.
Chen R, Fairley JA, Zhao M, Giudice GJ, Zillikens D, Diaz LA, et al. Macrophages, but not T and B lymphocytes, are critical for subepidermal blister formation in experimental bullous pemphigoid: macrophage-mediated neutrophil infiltration depends on mast cell activation. J Immunol 2002 -10-01;169(7):3987-3992.
Messingham KAN, Noe MH, Chapman MA, Giudice GJ, Fairley JA. A novel ELISA reveals high frequencies of BP180-specific IgE production in bullous pemphigoid. J Immunol Methods 2009 -07-31;346(1-2):18-25.
Zone JJ, Taylor T, Hull C, Schmidt L, Meyer L. IgE basement membrane zone antibodies induce eosinophil infiltration and histological blisters in engrafted human skin on SCID mice. J Invest Dermatol 2007 -05;127(5):1167-1174.
Amber KT, Chernyavsky A, Agnoletti AF, Cozzani E, Grando SA. Mechanisms of pathogenic effects of eosinophil cationic protein and eosinophil-derived neurotoxin on human keratinocytes. Exp Dermatol 2018 -12;27(12):1322-1327.
Messingham KN, Holahan HM, Frydman AS, Fullenkamp C, Srikantha R, Fairley JA. Human Eosinophils Express the High Affinity IgE Receptor, FcεRI, in Bullous Pemphigoid. PLoS One 2014 -9-25;9(9):e107725.
de Graauw E, Sitaru C, Horn M, Borradori L, Yousefi S, Simon H-, et al. Evidence for a role of eosinophils in blister formation in bullous pemphigoid. Allergy 2017 -07;72(7):1105-1113.
Verraes S, Hornebeck W, Polette M, Borradori L, Bernard P. Respective contribution of neutrophil elastase and matrix metalloproteinase 9 in the degradation of BP180 (type XVII collagen) in human bullous pemphigoid. J Invest Dermatol 2001 -11;117(5):1091-1096.
Ståhle-Bäckdahl M, Inoue M, Guidice GJ, Parks WC. 92-kD gelatinase is produced by eosinophils at the site of blister formation in bullous pemphigoid and cleaves the extracellular domain of recombinant 180-kD bullous pemphigoid autoantigen. J Clin Invest 1994 -05;93(5):2022-2030.
Kelly EAB, Liu LY, Esnault S, Quinchia Johnson BH, Jarjour NN. Potent synergistic effect of IL-3 and TNF on matrix metalloproteinase 9 generation by human eosinophils. Cytokine 2012 -05;58(2):199-206.
Wakugawa M, Nakamura K, Hino H, Toyama K, Hattori N, Okochi H, et al. Elevated levels of eotaxin and interleukin-5 in blister fluid of bullous pemphigoid: correlation with tissue eosinophilia. Br J Dermatol 2000 -07;143(1):112-116.
Bonciani D, Quintarelli L, Del Bianco E, Bianchi B, Caproni M. Serum levels and tissue expression of interleukin-31 in dermatitis herpetiformis and bullous pemphigoid. J Dermatol Sci 2017 -08;87(2):210-212.
Rüdrich U, Gehring M, Papakonstantinou E, Illerhaus A, Engmann J, Kapp A, et al. Eosinophils are a Major Source of Interleukin-31 in Bullous Pemphigoid. Acta Derm Venereol 2018 -08-29;98(8):766-771.
Borradori L, Van Beek N, Feliciani C, Tedbirt B, Antiga E, Bergman R, et al. Updated S2 K guidelines for the management of bullous pemphigoid initiated by the European Academy of Dermatology and Venereology (EADV). J Eur Acad Dermatol Venereol 2022 -10;36(10):1689-1704.
Russo R, Capurro N, Cozzani E, Parodi A. Use of Dupilumab in Bullous Pemphigoid: Where Are We Now? J Clin Med 2022 -6-12;11(12):3367.
Abdat R, Waldman RA, de Bedout V, Czernik A, Mcleod M, King B, et al. Dupilumab as a novel therapy for bullous pemphigoid: A multicenter case series. J Am Acad Dermatol 2020 -07;83(1):46-52.
Zeng FAP, Murrell DF. Bullous pemphigoid—What do we know about the most recent therapies? Frontiers in medicine 2022 Nov 3,;9:1057096.
Simon D, Yousefi S, Cazzaniga S, Bürgler C, Radonjic S, Houriet C, et al. Mepolizumab failed to affect bullous pemphigoid: A randomized, placebo-controlled, double-blind phase 2 pilot study. Allergy 2020 -03;75(3):669-672.
Rhyou H, Han S, Nam Y. Successful induction treatment of bullous pemphigoid using reslizumab: a case report. Allergy Asthma Clin Immunol 2021 -11-16;17(1):117.
Dagher R, Kumar V, Copenhaver AM, Gallagher S, Ghaedi M, Boyd J, et al. Novel mechanisms of action contributing to benralizumab's potent anti-eosinophilic activity. Eur Respir J 2022 -03;59(3):2004306.
Cómo citar
Descargas
Publicado
Cómo citar
Número
Sección
Licencia
Derechos de autor 2025 Artur Moraes-L'Abbate, Carolina Cortés Correa

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial-CompartirIgual 4.0.
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |